お知らせ
2026年4月
・荒谷さん(M1)がグループに参加しました。Welcome!!(2日)
・大西さんがCold Spring Harbor Conferences Asiaでポスター発表をします(中国・蘇州, 7日)。
・18日土曜日の午後1時から大学院進学説明会があります。ぜひご参加ください。
下記URLから登録するとZoomのリンクが送られてきます。
https://u-tokyo-ac-jp.zoom.us/meeting/register/utX-gCeHSKihbuS3L3fJeA
2026年2月
・第22回成体脳のニューロン新生懇談会で大西さんと木原くんが口頭発表・ポスター発表をしました(高
知, 28日)。木原くんがYoung Investigator Award(口頭)を受賞しました。Congratulations!!
2025年12月
・Zhangくんの論文がbioRxivに公開されました(17日)。
2025年11月
・京都での生化学会に参加し、大西さんがポスター発表、小林がシンポジウムオーガナイザーと口頭発表
を行いました(4日)。
・研究所のソフトボール大会がありました(12日)。
・第 19 回日本臨床ストレス応答学会大会で小林が口頭発表を行いました(14日金沢)。
2025年10月
・研究生としてギさん、Williamくんがグループに参加しました。Welcome!!
・Dieter Chichung Lie教授がラボを訪問してくれました(28日)。
・奈良での国際会議ISPO2025に参加し、Chuiくん、大西さん、木原くん、新田くん、Zhangくんがポス
ター発表、小林が口頭発表を行いました(30日〜11月2日)。
2025年9月
・第68回日本神経化学会大会で新田くん、Zhangくんがポスター発表、小林が招待講演を行いました。
(11-13日名古屋)
・Zhangくんが京都大学生命科学研究科の修士課程を修了しました。Congratulations! (24日)
2025年7月
・ラボローテーションでALVINくんが来てくれました。Welcome!
・Spring GX General Meetingで大西さん、木原くん、新田くんがポスター発表をしました(12日)。
2025年5月
・学術変革領域「蛋白質寿命」が主催する国際シンポジウム「ISPO2025」の参加登録が始まりました
(2025年10月30日〜11月2日、奈良春日野フォーラム)。https://ispo2025.f.u-tokyo.ac.jp/
・木原くんが第52回医科学研究所創立記念シンポジウムでFlash talk(29日)とポスター発表(30日)を
行いました。Translational Regulation for Quiescence of Neural Stem Cells
はじめに
1つの細胞である受精卵から生み出された私たちの体は、約210種類、計37兆個もの細胞で構成されています。体の中では、幹細胞が新しく細胞を作り、常に細胞を入れ替えて体の機能を維持しています。
近年、脳の中にも幹細胞(神経幹細胞)が一生涯に渡って存在し、神経細胞(ニューロン)を新しく作り出せることがわかってきました。
しかし、大人の脳の中の神経幹細胞のほとんどは眠っている(休眠)状態にあります。この眠っている神経幹細胞は、どのように脳の機能維持に関わっているのでしょうか?
私たちのグループでは、神経幹細胞の休眠制御のメカニズムに興味をもって現在、研究を進めています。

研究内容
体の中に存在する幹細胞は、組織内の適切な環境(ニッチ)に限局して存在しています。大人の脳組織に存在する成体神経幹細胞も、脳室周囲と海馬の歯状回に限局して存在し、細胞内や細胞外環境から様々な制御を受けています。
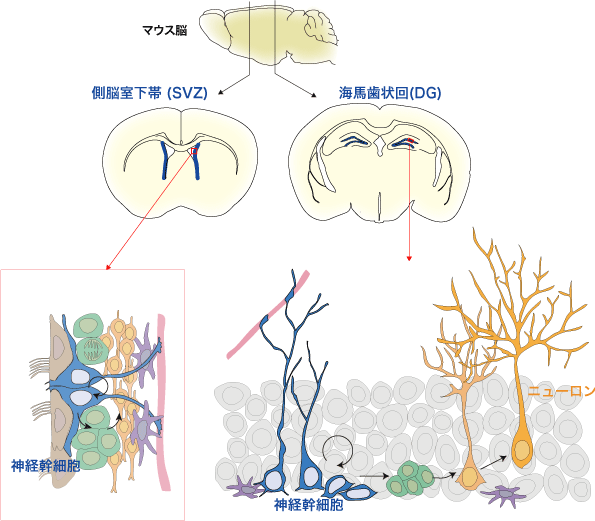
私たちは、最近、細胞内の不要な物質を分解処理する細胞小器官である「リソソーム」が、神経幹細胞の「休眠」を制御していることを見出しました(Kobayashi et al (2019))。
「休眠」とは、増殖も分化もせずに幹細胞としての機能を停止している状態(細胞周期でのG0期)であり、長期間にわたる幹細胞の維持に必要だと考えられています。活性化されると機能を取り戻します。成体内の90%を超える神経幹細胞が、休眠状態にあると言われています。
「リソソーム」は、細胞内の不要な物質の分解処理を行うだけでなく、細胞内の栄養状態を感知し、細胞内のタンパク質や脂質の状態を整えたり、分泌により細胞外の環境を変えたり、様々な役割を持っています。
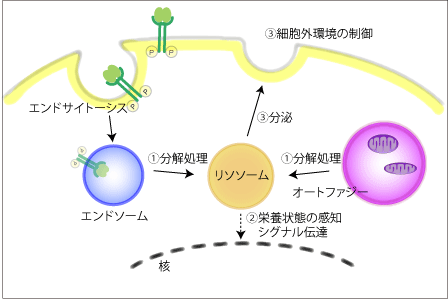
私達は現在、神経幹細胞におけるリソソームの機能に着目をした解析と、物理学的な特性である固さ(弾性率:stiffness)による制御に着目した解析を行っています。
次の項目について、解析を進めています。
-
細胞外からの休眠シグナルとリソソームをつなぐ経路とその制御
-
細胞内で休眠状態を制御しているタンパク質恒常性等の制御
-
リソソームを介した細胞外の微小環境制御
-
細胞外の力学的な特性による神経幹細胞制御
これらの研究成果から、脳機能の維持における神経幹細胞の休眠制御について、明らかにしていきます。

最近の研究成果
Zhang, H., Kihara, Y., Sasaki, M., Tomita, T., Saeki, Y. and *Kobayashi, T.
Caveolin-1 controls lineage fidelity of adult neural stem cells via lysosomal degradation of PDGFRα
bioRxiv (2025)
https://doi.org/10.64898/2025.12.16.694780
Zhang, H., Ishii, K., Shibata, T., Ishii, S., Hirao, M., Lu, Z., Takamura, R., Kitano, S., Miyachi, H., Kageyama, R., Itakura, E. and *Kobayashi, T.
Fluctuation of lysosomal protein degradation in neural stem cells of postnatal mouse brain
Development. 151, dev202231 (2024)
https://doi.org/10.1242/dev.202231
Park, G., Shin, M., Lee, W. Hotta, A., Kobayashi, T. and *Kosodo, Y.
Direct visualization of the transition status during neural differentiation by dual-fluorescent reporter human pluripotent stem cells.
Stem Cell Reports. 17, 1903-1913. (2022)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9481873/
Kaise, T., Fukui, M., Sueda, R., Piao, W., Yamada, M., Kobayashi, T., Imayoshi, I. and *Kageyama, R.
Functional rejuvenation of aged neural stem cells by Plagl2 and anti-Dyrk1a activity.
Genes Dev. 36, 23-37. (2022)
http://genesdev.cshlp.org/content/early/2021/12/14/gad.349000.121
Zhang, J., Uchiyama, J., Imami, K., Ishihama, Y., Kageyama, R. and *Kobayashi,T.
Novel roles of small extracellular vesicles in regulating the quiescence and proliferation of neural stem cells.
Frontiers in Cell and Developmental Biology 9 | Article 762293 (2021)
https://www.frontiersin.org/articles/10.3389/fcell.2021.762293
*Kobayashi, T. and *Kageyama, R.
Lysosomes and signaling pathways for maintenance of quiescence in adult neural stem cells.
FEBS J. 288, 3082-3093. (2020) State‐of‐the‐Art Review
https://doi.org/10.1111/febs.15555
*Kobayashi, T., Piao, W., Takamura, T., Kori, H., Miyachi, H., Kitano, S., Iwamoto, Y., Yamada, M., Imayoshi, I., Shioda, S., Ballabio, A., and *Kageyama, R.
Enhanced lysosomal degradation maintains the quiescent state of neural stem cells.
Nat. Commun. 10, 5446. (2019)
メンバー
卒業生
お問い合わせ
小林 妙子
〒108-8639
東京都港区白金台4-6-1
東京大学医科学研究所 基礎医科学部門 タンパク質代謝制御分野
総合研究棟5F 5203
TEL:03-5449-5257(直通)
*東京大学医学系研究科、薬学研究科の大学院生を受け入れています。



















